La politique, la science et la remarquable course pour un vaccin contre les coronavirus
La politique, la science et la remarquable course pour un vaccin
La course effrénée pour le développement d’un vaccin contre les coronavirus s’est jouée contre une élection présidentielle, entre un géant pharmaceutique et un débutant en biotechnologie, avec des enjeux aussi élevés que possible.
 Stéphane Bancel, le directeur général de Moderna, a accepté de s’associer au gouvernement fédéral pour développer un vaccin, un partenariat qui a permis d’éviter l’ingérence politique de la Maison Blanche qui avait entravé d’autres efforts pour lutter contre le virus.
Stéphane Bancel, le directeur général de Moderna, a accepté de s’associer au gouvernement fédéral pour développer un vaccin, un partenariat qui a permis d’éviter l’ingérence politique de la Maison Blanche qui avait entravé d’autres efforts pour lutter contre le virus.
WASHINGTON – 21 novembre 2020
L’appel était tendu, le message décourageant. Moncef Slaoui, responsable de l’effort de l’administration Trump pour produire rapidement un vaccin contre le coronavirus, était au téléphone le 25 août à 18 heures pour dire à la jeune entreprise de biotechnologie Moderna qu’elle devait ralentir la dernière étape des tests de son vaccin chez l’homme.
Le directeur général de Moderna, Stéphane Bancel, un ingénieur biochimiste français, a reconnu l’implication. Dans la course à la lutte contre la pandémie, il a déclaré que « chaque jour comptait ». Sa société, qui n’avait pas encore mis un seul produit sur le marché, a dû faire face à un retard pouvant aller jusqu’à trois semaines. Pfizer, le géant pharmaceutique mondial qui était occupé à tester un candidat vaccin similaire et qui promettait de premiers résultats pour octobre, allait prendre la tête du peloton.
« C’est la décision la plus difficile que j’ai prise cette année », a déclaré M. Bancel.
Le problème de Moderna semblait se poser à la fin de l’été 2020, alors que les États-Unis étaient sous le coup non seulement d’une pandémie, mais aussi de troubles liés à l’injustice raciale. Le Dr Slaoui a informé M. Bancel que Moderna n’avait pas recruté suffisamment de candidats issus des minorités dans ses essais de vaccins. S’il ne pouvait pas prouver que son vaccin fonctionnait bien pour les Noirs et les Hispano-Américains, qui ont été touchés de manière disproportionnée par la pandémie, il ne franchirait pas la ligne d’arrivée.
Les deux sociétés ont finalement achevé les étapes cruciales de leurs essais sur l’homme ce mois-ci et ont fait état de premiers résultats spectaculaires, des vaccins qui semblent être efficaces à environ 95 % contre un virus qui a tué 1,3 million de personnes, dont un quart de million aux États-Unis.
Peu de compétitions entre entreprises se sont déroulées avec des enjeux aussi importants et un contexte aussi complexe. Il ne s’agissait pas seulement de rivalités commerciales et de défis scientifiques, mais aussi d’un plan ambitieux visant à mettre le gouvernement fédéral au centre de l’effort et, ce qui est le plus vexant, de l’atmosphère politique souvent toxique créée par le président Trump. Pariant qu’un vaccin garantirait sa réélection, il a mené des campagnes publiques et privées pour accélérer le processus.
Le directeur général de Pfizer, le Dr Albert Bourla, avait juré d’éviter le champ de mines politique, mais il a néanmoins été contraint de le traverser. Après avoir promis des progrès sur un calendrier qui semblait soutenir la prédiction de M. Trump d’une percée avant le jour de l’élection, le Dr Bourla a repoussé le calendrier à la fin octobre, craignant que les résultats des essais cliniques de sa firme ne soient pas suffisamment convaincants pour que les régulateurs fédéraux accordent une approbation d’urgence à son vaccin. La nouvelle du succès de Pfizer a été annoncée juste après le déclenchement de l’élection de Joseph R. Biden Jr.
Le Dr Bourla avait choisi dès le départ de maintenir Pfizer et son partenaire de recherche, la firme allemande BioNTech, à l’écart du gouvernement, en raison de la diminution des fonds consacrés à la recherche et au développement dans le cadre de l’opération fédérale de sauvetage, appelée Operation Warp Speed.
M. Bancel, avec une entreprise beaucoup plus petite, a fait le pari inverse, en acceptant l’aide d’un gouvernement dirigé par un président qui nie la science. Moderna a obtenu près de 2,5 milliards de dollars pour développer, fabriquer et vendre son vaccin au gouvernement fédéral et a fait équipe avec les Instituts nationaux de la santé pour les travaux scientifiques, un partenariat très fructueux qui a réussi à éviter l’ingérence politique de M. Trump et de ses assistants qui avaient entravé d’autres efforts pour lutter contre le virus.
Pfizer et Moderna ne pourraient à eux seuls répondre à la demande nationale ou mondiale, mais d’autres entreprises aux États-Unis et dans le monde entier se précipitent également vers des vaccins efficaces, dont certains utilisent des technologies plus éprouvées, de sorte que d’autres gagnants sont susceptibles d’émerger.
Pourtant, les deux sociétés, à leur manière très différente, ont réussi un exploit remarquable : mettre au point un vaccin qui semble sûr et efficace en quelques mois, plutôt qu’en quelques années ou décennies comme c’est généralement le cas. Elles ont été aidées par la confluence de trois facteurs. Une nouvelle méthode de développement des vaccins attendait déjà d’être testée, le coronavirus étant une cible parfaite. Les taux d’infection très élevés ont accéléré le rythme des essais cliniques, la partie la plus longue du processus. Et le gouvernement était prêt à dépenser tout ce qu’il fallait, en éliminant les risques financiers et les obstacles bureaucratiques et en permettant le démarrage de la production de masse avant même que les essais ne soient terminés.
Leur succès apparent a montré qu’à une époque de polarisation politique, la science était capable de faire tomber les barrières entre le gouvernement, les pays et l’industrie pour produire l’une des rares bonnes nouvelles en une année de souffrance et de division.
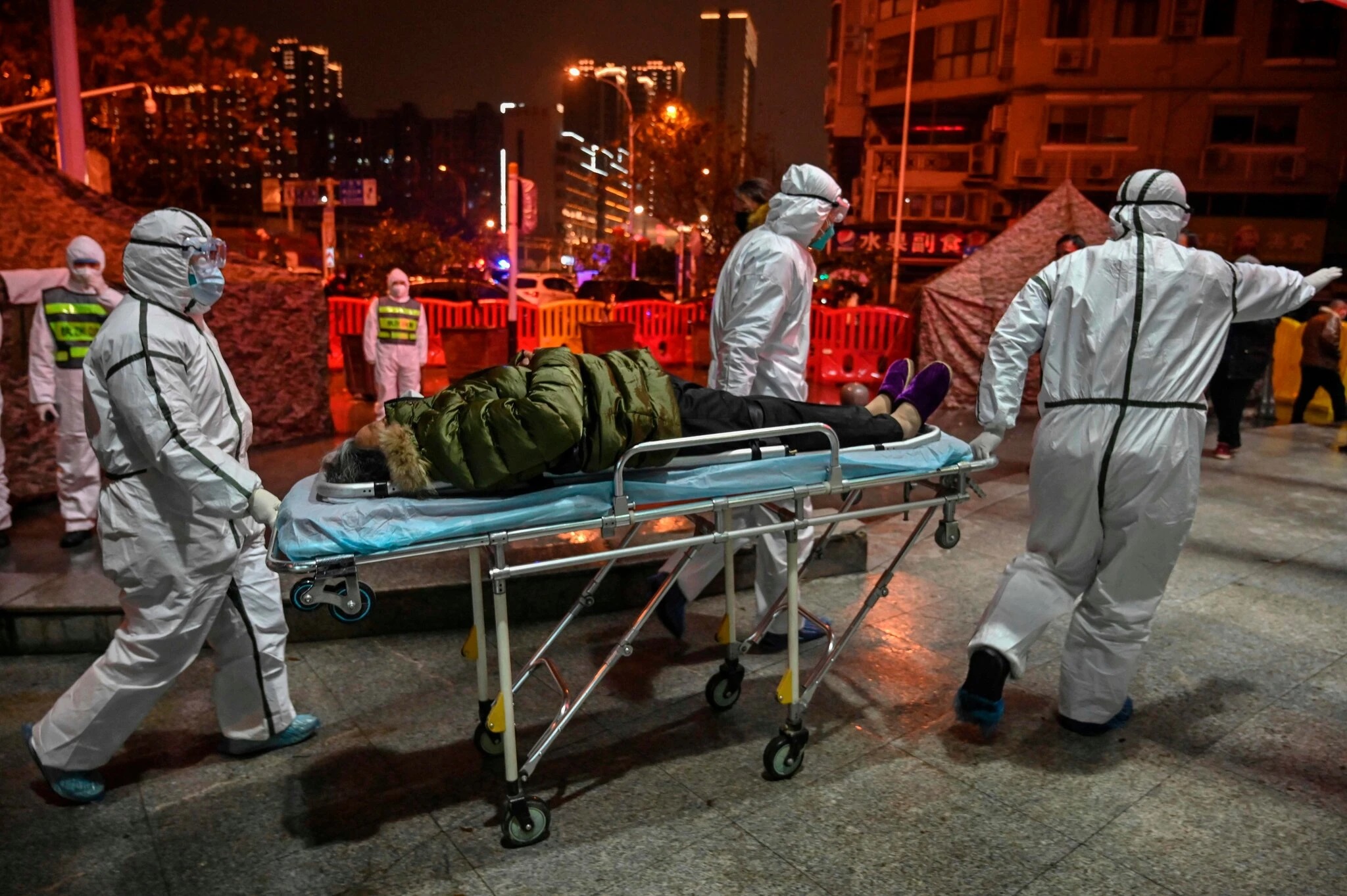 L’épidémie qui s’est répandue en Chine en janvier présentait les caractéristiques d’une pandémie prolongée.
L’épidémie qui s’est répandue en Chine en janvier présentait les caractéristiques d’une pandémie prolongée.
Credit: Hector Retamal/Agence France-Presse – Getty Images
Etes-vous sûr que nous devrions faire cela ?
M. Bancel était en Suisse pour une conférence d’affaires en janvier quand il a entendu parler d’une nouvelle épidémie virale mortelle à Wuhan, en Chine. Il a immédiatement pris contact avec deux experts en vaccins du N.I.H. avec lesquels sa société travaille depuis des années pour développer une technologie qui pourrait être utilisée pour concevoir des vaccins, une sorte de système prêt à l’emploi qui révolutionnerait la manière dont l’humanité fait face aux nouveaux agents pathogènes.
Si les systèmes fonctionnaient, la conception d’un vaccin se ferait en quelques jours. La tâche restante consisterait à procéder à de longs essais pour s’assurer que le vaccin fonctionne et est sûr, un processus qui ne connaît aucun raccourci.
Contrairement aux méthodes plus anciennes et plus lentes de développement des vaccins, qui consistent à stimuler le système immunitaire de l’organisme en injectant des virus inactivés ou affaiblis, Moderna et d’autres entreprises ont créé des plateformes qui fonctionnent comme le système d’exploitation d’un ordinateur, permettant aux chercheurs d’insérer rapidement le nouveau code génétique d’un virus – comme l’ajout d’une application – et de créer un nouveau vaccin.
La méthode utilise une forme synthétique d’une molécule génétique appelée ARN messager, ou ARNm, pour amener les cellules humaines à fabriquer une protéine virale inoffensive appelée « pic », qui stimule ensuite le système immunitaire à fabriquer des anticorps et des cellules immunitaires capables de reconnaître rapidement le pic et de contre-attaquer si nécessaire.
Les efforts déployés précédemment pour tester de nouveaux types de vaccins dans des épidémies comme le SRAS, le MERS et le Zika avaient échoué lorsque la menace de ces virus s’est estompée, avant que de grands essais cliniques puissent être réalisés. Mais l’épidémie qui s’est répandue en Chine avait les caractéristiques d’une pandémie prolongée, une tragédie mais aussi un terrain d’essai parfait pour la nouvelle biotechnologie.
M. Bancel, 48 ans, avait ce qu’un ancien collègue a décrit comme une « personnalité guerrière ». Il avait quitté une entreprise beaucoup plus importante pour devenir directeur général de Moderna en 2011, avertissant sa femme que le pari de l’ARNm de l’entreprise avait 5 % de chances de réussir. Mais si ce pari s’avérait payant, lui a-t-il dit, cela changerait le cours de la médecine.
Fin 2019, a-t-il dit, le Centre de recherche sur les vaccins du NIH a accepté de mettre en place une sorte de jeu de guerre au printemps suivant, une simulation de pandémie avec un virus inconnu de Moderna pour voir à quelle vitesse la société pourrait mettre au point un vaccin.
Maintenant qu’une véritable pandémie est à portée de main, M. Bancel a voulu tester l’approche de Moderna pour de vrai.
Il a décrit la réaction de son équipe comme suit : « C’est reparti. Il est fou ».
« Vous êtes sûr qu’on devrait faire ça ? » lui a demandé le Dr Stephen Hoge, le président de la société, lors d’une réunion du comité exécutif en février.
Moderna n’employait que 800 personnes, dont une équipe de fabrication. Vingt vaccins et traitements étaient en cours de développement, mais aucun ne devait être commercialisé avant au moins deux ans. Elle n’avait jamais réalisé d’essai clinique de phase 3, c’est-à-dire les essais de dernière étape destinés à déterminer si un vaccin est sûr et efficace pour l’homme.
Certains dirigeants de Moderna ont suggéré de tester un vaccin pendant quelques mois, puis de le réévaluer. Mais Juan Andres, le directeur des opérations techniques et de la qualité de la société, a déclaré qu’il avait lancé un avertissement : « Désolé, les gars, il n’y a pas de sortie sur cette autoroute. Si nous sommes dedans, nous sommes dedans ».
Le N.I.H. est entré avec eux. Le Dr John R. Mascola, directeur du centre de recherche sur les vaccins, et le Dr Barney Graham, directeur adjoint du centre, ont proposé le partenariat au Dr Anthony S. Fauci, directeur de l’Institut national des allergies et des maladies infectieuses.
« Allez-y », leur a dit le Dr Fauci. « Quoi qu’il en coûte, ne vous inquiétez pas. »
L’objectif de Moderna était de passer de la conception d’un vaccin à un essai sur l’homme en trois mois. La conception s’est faite rapidement. « Ce n’est pas un virus compliqué », a déclaré M. Bancel.
Le Dr Graham a déclaré qu’après que la Chine ait publié la séquence génétique du nouveau virus, le centre de recherche sur les vaccins s’est concentré sur le gène de la protéine de pointe du virus et a envoyé les données à Moderna dans un fichier Microsoft Word. Les scientifiques de Moderna avaient indépendamment identifié le même gène. M. Bancel a déclaré que Moderna avait ensuite branché ces données sur ses ordinateurs et avait conçu un vaccin à ARNm. L’ensemble du processus a pris deux jours.
Les scientifiques du N.I.H. étaient « très chauds » sur l’approche ARNm, a déclaré le Dr Fauci. Mais Moderna n’était pas le seul.
 Avant la pandémie, Moderna n’avait jamais mené d’essai clinique de phase 3, c’est-à-dire les essais de dernière étape destinés à déterminer si un vaccin est sûr et efficace pour l’homme. Credit: Cody O’Loughlin
Avant la pandémie, Moderna n’avait jamais mené d’essai clinique de phase 3, c’est-à-dire les essais de dernière étape destinés à déterminer si un vaccin est sûr et efficace pour l’homme. Credit: Cody O’Loughlin
En Allemagne, les scientifiques Ugur Sahin et Özlem Türeci, mari et femme, ont suivi la même voie. Leur entreprise, BioNTech, travaillait depuis plusieurs années avec Pfizer pour développer un nouveau vaccin contre la grippe avec la même technologie d’ARNm que celle utilisée par Moderna. Le Dr Sahin a déclaré avoir demandé à un cadre de Pfizer, le 1er mars, si la société voulait se lancer dans la recherche d’un vaccin contre les coronavirus.
Briefing sur les coronavirus :
Un guide éclairé sur l’épidémie mondiale, avec les derniers développements et les conseils d’experts.
Le Dr Bourla, cadre supérieur de Pfizer, a concédé que lorsque le virus est apparu, il « n’avait pas l’impression à l’époque que cela deviendrait un problème mondial majeur qui nécessiterait une intervention majeure de notre part ».
Né en Grèce, vétérinaire de formation, il a gravi les échelons pendant plus de deux décennies, passant de la division de la santé animale de Pfizer au bureau du directeur général en 2019. Au départ, ce cadre de 59 ans s’est surtout concentré sur la protection des 90 000 employés de l’entreprise dans le monde entier.
Mais dès qu’il a appris la proposition des Allemands, lui et sa société ont agi rapidement. Pfizer a accepté de prendre en charge les coûts de développement de BioNTech et de gérer les essais cliniques, la fabrication et la distribution. BioNTech a accepté de rembourser Pfizer sur les bénéfices éventuels, qui seraient partagés.
Certains collègues du Dr Sahin lui ont conseillé d’attendre un contrat officiel avant de donner à Pfizer des données sur le vaccin. Le Dr Sahin a répondu qu’il n’y avait « pas de temps à perdre ». Pfizer a envoyé son jet d’entreprise en Allemagne pour transporter des échantillons du vaccin BioNTech au centre de recherche de la société à Pearl River, N.Y., pour commencer à le tester sur des animaux.
« Pour Pfizer, il s’agit autant de relations publiques que de rendement financier – ils veulent vraiment être considérés comme faisant partie de la solution », a déclaré Geoffrey Porges, un analyste de SVB Leerink, une banque d’investissement à Boston.
« Pour Moderna », a-t-il dit, « c’est en fait une énorme opportunité de validation ».
 Le vice-président Mike Pence et le président Trump font le point sur l’opération Warp Speed dans la roseraie ce mois-ci. Credit: Anna Moneymaker.
Le vice-président Mike Pence et le président Trump font le point sur l’opération Warp Speed dans la roseraie ce mois-ci. Credit: Anna Moneymaker.
L’opération Warp Speed est née.
Alors que l’économie s’est arrêtée au printemps dernier et que les décès se sont multipliés à New York, Detroit et Chicago, les responsables de l’administration ont proposé un effort coordonné pour mettre au point des tests, des traitements et des vaccins pour ce qui était désormais clairement la plus grave crise de santé publique depuis un siècle.
L’opération Warp Speed a été conçue par le Dr Peter Marks, le principal responsable de la réglementation des vaccins pour la Food and Drug Administration. Fruit d’une collaboration entre le Pentagone et le ministère de la santé et des services sociaux, elle a été conçue pour soutenir les entreprises pharmaceutiques et biotechnologiques grâce à toute l’étendue de l’expertise du gouvernement, des essais cliniques à la logistique. L’objectif pour un vaccin était le mois d’octobre, selon une note préliminaire.
Le président s’est montré particulièrement enthousiaste à l’égard de cet objectif. Lors d’une réunion à la Maison Blanche le 2 mars, alors que M. Bancel et d’autres dirigeants de l’industrie pharmaceutique exposaient leurs projets de vaccins, le Dr Fauci a averti qu’il faudrait attendre « un an à un an et demi » avant que les doses puissent atteindre le grand public.
M. Trump a répondu : « Je préfère le son d’un couple de quelques mois ».
Warp Speed avait deux leaders. Le Dr Slaoui, responsable de la science, avait dirigé la recherche et le développement chez le fabricant de médicaments GlaxoSmithKline pendant des années et avait siégé au conseil d’administration de Moderna. Le responsable de la logistique était le général Gustave F. Perna, un général quatre étoiles qui dirigeait le commandement du matériel de l’armée.
L’opération, qui s’est déroulée dans une suite au septième étage et dans un centre d’opérations au deuxième étage du quartier général de la santé et des services sociaux, avait une saveur militaire. Ses dirigeants ont discuté du livre « Freedom’s Forge », un récit sur la façon dont l’industrie américaine a armé l’armée pendant la Seconde Guerre mondiale, et ont imposé ce qu’ils ont appelé un « rythme de bataille » de réunions, y compris une séance quotidienne de 8 heures sur les vaccins. Des dizaines d’officiers militaires ont déclaré travailler en uniforme.
La décision la plus importante, selon le Dr Slaoui, a été de choisir les candidats vaccins à écarter parmi près de 50 candidats possibles. Son équipe a choisi trois types de vaccins, chacun devant être poursuivi par deux sociétés en cas d’échec de l’une d’entre elles. Les fonctionnaires fédéraux ont qualifié les finalistes de « chevaux », un clin d’œil à la course entre eux.
Moderna et Pfizer poursuivraient les vaccins à ARNm, considérés comme les plus rapides à développer. Le gouvernement était prêt à payer une grande partie de la facture du développement, à guider les essais cliniques et même à livrer des fournitures aux usines.
Le Dr Bourla n’était pas intéressé. En tant que l’un des principaux producteurs de vaccins au monde, Pfizer n’avait pas besoin de l’aide fédérale pour développer un nouveau produit, décida-t-il, et avec près de 52 milliards de dollars de revenus annuels, elle n’avait pas besoin ou ne voulait pas de cette subvention.
« Si nous ne réussissions pas, nous devrions amortir 2 milliards de dollars » de coûts de développement de vaccins, a déclaré le Dr Bourla lors du sommet en ligne sur les livres de transaction du New York Times cette semaine. « C’est douloureux pour toute entreprise, mais cela n’allait pas nous briser. »
Lors d’une interview vendredi, il a déclaré qu’il craignait que la surveillance du gouvernement ne ralentisse le travail de son entreprise, et non ne l’accélère. Et il craignait que le financement fédéral ne soit assorti de conditions.
« Je n’avais pas l’impression que je voulais finir par entrer dans le débat politique, ce que je ne suis pas sûr d’avoir pu éviter en ne prenant pas d’argent », a déclaré le Dr Bourla. « Mais si j’avais pris de l’argent, cela aurait été bien pire ».
Pfizer a signé un accord de 1,95 milliard de dollars en juillet pour vendre au gouvernement fédéral 100 millions de doses de son vaccin en cas de succès, lui garantissant un acheteur, ce qui n’est pas une mince incitation. Elle a également fait appel à plusieurs reprises à l’administration Trump pour avoir accès aux fournitures de fabrication. Sinon, elle s’est débrouillée seule.
Moderna n’avait aucun scrupule à demander l’aide du gouvernement. « Les gars, nous n’avons pas un bilan comme celui de Pfizer », a déclaré M. Bancel aux fonctionnaires fédéraux.
Près de 2,5 milliards de dollars de fonds fédéraux ont permis à Moderna d’acheter des matières premières, d’agrandir son usine et d’augmenter sa main-d’œuvre de 50 %. En retour, elle a promis de livrer 100 millions de doses au gouvernement fédéral.
Elle a également bénéficié d’une expertise. L’opération Warp Speed a permis de créer six équipes d’une quinzaine de spécialistes des essais cliniques, d’épidémiologistes et d’experts budgétaires, chacune étant affectée à un fabricant de vaccins différent.
Les hauts responsables ont organisé des réunions hebdomadaires avec les responsables des essais cliniques des entreprises, en suivant le recrutement des participants aux essais et en couvrant les tableaux blancs de plans de distribution potentiels.
L’équipe de Moderna était dirigée par un fonctionnaire du ministère de la défense que les dirigeants de l’entreprise n’ont décrit que comme « le major », disant qu’ils ne savent pas si son nom est censé être un secret. Un haut responsable de Warp Speed a décrit une atmosphère de « terreur totale » à propos d’une poussée d’infections à la fin de l’automne et en hiver. Dans un scénario apocalyptique envisagé par les responsables, une épidémie dans une usine de Covid-19 pourrait gâcher trois mois de doses de vaccin.
Lorsque Moderna a découvert cet été qu’une unité de traitement de l’air pour son usine ne pouvait pas être livrée en un week-end en raison des limitations de Covid-19 sur le transport routier inter-États, l’équipe du major est intervenue. Les responsables de Warp Speed ont organisé une escorte des forces de l’ordre pour accompagner l’énorme pièce d’équipement du Midwest à son usine du Massachusetts.
L’équipe est à nouveau entrée en action lorsque Moderna a découvert qu’une pompe spécialisée, nécessaire à la fabrication des premiers lots de vaccins pour les essais cliniques, était bloquée dans un wagon et n’allait pas être livrée à temps. Des employés fédéraux ont suivi le train et l’ont fouillé jusqu’à ce qu’ils trouvent la pompe.
« Ils l’ont mise dans un avion et elle est arrivée à temps », a déclaré M. Andres, le chef des opérations de la société.
Les interventions, a-t-il dit, ont été « absolument déterminantes ».
 Des voitures font la queue sur un site de test à Mandan, N.D., mercredi. Le virus continue de ravager le Midwest. Credit: Tim Gruber.
Des voitures font la queue sur un site de test à Mandan, N.D., mercredi. Le virus continue de ravager le Midwest. Credit: Tim Gruber.
Nous devions parler.
Au début de l’automne, les pressions politiques qui s’étaient accumulées toute l’année ont éclaté au grand jour. Les régulateurs fédéraux essayaient de publier des directives pour assurer un suivi suffisant des participants aux essais cliniques afin de garantir la sécurité des vaccins, mais les responsables de la Maison Blanche les bloquaient. Le président s’en prenait aux responsables de la F.D.A., qu’il considérait comme des antagonistes désireux de contrecarrer sa réélection.
Le Dr Bourla avait été entraîné dans le bosquet politique, en partie à cause de ses propres promesses selon lesquelles Pfizer attendait des résultats d’essais cliniques pour octobre. Le président a repoussé cette échéance dans le cadre de sa campagne et a tenté de se lier publiquement au dirigeant de Pfizer.
Le Dr Sahin, de BioNTech et partenaire de Pfizer, a déclaré que le Dr Bourla essayait de gérer « une situation inconfortable ». Mais lorsque le président s’en est pris à la F.D.A., le Dr Bourla a tiré un trait, décidant que la confiance du public dans un vaccin était en jeu. « Nous avons fait des déclarations contre la FDA, l’État profond, etc., qui m’inquiétaient vraiment », a-t-il déclaré. « Nous devions nous exprimer. »
Il a appelé Alex Gorsky, le directeur général de Johnson & Johnson, un autre concurrent de premier plan dans la course au vaccin, puis a recruté des dirigeants d’autres sociétés. Ensemble, ils ont rédigé une déclaration qui disait que l’industrie « se tiendrait à la science » et suivrait les directives de la FDA. Le 8 septembre, neuf entreprises, dont Moderna, avaient signé la déclaration.
Dans le même temps, des problèmes de conception et d’exécution des essais cliniques sont apparus. Pfizer et Moderna étaient toutes deux confrontées au problème du nombre insuffisant de volontaires minoritaires, mais Pfizer avait les moyens de le résoudre. L’entreprise a étendu son essai de 30 000 à 44 000, une décision qui, selon le Dr Eric Topol, expert en essais cliniques chez Scripps Research à La Jolla, en Californie, a coûté à l’entreprise des centaines de millions de dollars.
Lorsque le Dr Slaoui, de l’opération Warp Speed, a appelé le directeur général de Moderna pour lui dire que l’entreprise devait recruter davantage de membres des minorités, cela a été un coup dur. Le Dr. Slaoui l’a dit à un collègue par la suite : « Je viens de brûler toutes nos relations » avec Moderna.
Le Dr Fauci a rencontré les chercheurs de l’essai de Moderna et a fait appel à des experts du NIH pour aider la société à atteindre davantage de volontaires noirs et hispaniques. Si Moderna a été saluée pour la diversification de son pool, Pfizer, dont l’essai était déjà conçu pour atteindre un résultat plus rapidement que celui de Moderna, était désormais incontestablement en tête.
Mais Pfizer a dû faire face à sa propre crise.
 Chercheur au Centre de virologie et de recherche sur les vaccins du Beth Israel Deaconess Medical Center à Boston. Le centre a développé un vaccin contre les coronavirus avec Johnson & Johnson. Crédit: Tony Luong.
Chercheur au Centre de virologie et de recherche sur les vaccins du Beth Israel Deaconess Medical Center à Boston. Le centre a développé un vaccin contre les coronavirus avec Johnson & Johnson. Crédit: Tony Luong.
Dans un essai clinique en double aveugle, l’étalon-or pour tester de nouveaux médicaments ou vaccins, ni la société ni les participants ne savent qui reçoit les vaccins et qui reçoit les placebos. Seul un comité d’examen indépendant a accès à ces informations.
Les protocoles des essais précisent dans quelles conditions le conseil peut examiner les résultats. Le protocole d’essai de Pfizer était le plus agressif des six candidats vaccins, ce qui a permis de vérifier les résultats intermédiaires une fois que 32 participants ont développé Covid-19.
Il constituait un point de référence inférieur à celui adopté par Moderna et les autres sociétés, et les autorités réglementaires de la FDA ont averti Pfizer qu’il était très peu probable qu’elles délivrent une autorisation d’utilisation d’urgence pour un vaccin contre les coronavirus sur la base d’un ensemble de données aussi restreint. Des experts externes ont critiqué Pfizer pour s’être permis de jeter un coup d’œil sur les données trop tôt et trop souvent.
Pfizer a décidé d’abandonner ce premier critère et a demandé à la FDA d’approuver un nouveau protocole le 29 octobre, anéantissant ainsi les espoirs de M. Trump d’une annonce avant le jour des élections.
La société a également cessé de traiter les résultats des tests des participants aux essais pendant qu’elle travaillait avec la F.D.A. Les changements de protocole sont découragés une fois que les données sont disponibles, et Pfizer ne voulait pas franchir le seuil avant d’avoir obtenu l’approbation verbale de l’abandonner. Cette approbation est intervenue le 3 novembre, le jour du scrutin, ou le lendemain.
Le retard a ensuite mis M. Trump en colère, qui a affirmé que cela faisait partie d’une conspiration visant à compromettre ses chances de réélection. Le Dr Bourla a déclaré qu’il avait fermé les yeux sur l’échéance du jour du scrutin.
« Avant, les gens disaient que c’était trop tôt », a-t-il dit. Après l’élection, « les gens disent : ‘Oh, c’est trop tard' ».
Une fois que Pfizer a repris le traitement des prélèvements de test le 4 novembre, il est rapidement devenu évident que le taux d’infection était monté en flèche, comme il l’avait fait à l’échelle nationale et dans d’autres pays.
Avec 94 cas Covid-19, la société a demandé au conseil de surveillance des données de révéler les résultats.
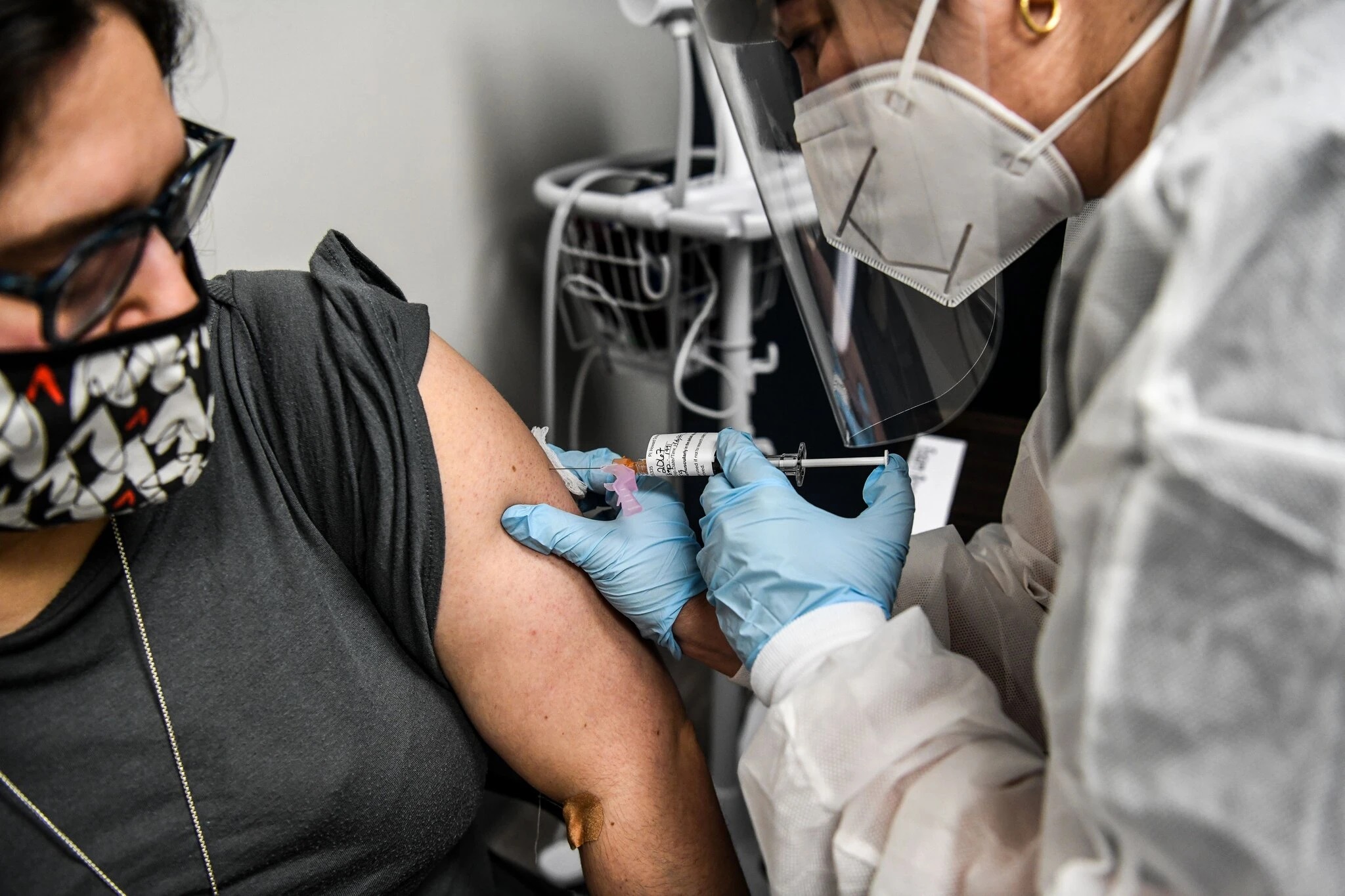 Heather Lieberman, 28 ans, participe à un essai de vaccin contre les coronavirus aux Research Centers of America à Hollywood, en août. Crédit: Chandan Khanna/Agence France-Presse – Getty Images
Heather Lieberman, 28 ans, participe à un essai de vaccin contre les coronavirus aux Research Centers of America à Hollywood, en août. Crédit: Chandan Khanna/Agence France-Presse – Getty Images
Silence assourdissant, puis étreintes et larmes
Le dimanche matin 8 novembre, le Dr Bourla se rendit au bureau de Pfizer à Cos Cob, dans le Connecticut, pour entendre le verdict avec quelques collaborateurs de haut niveau. « Je ne pouvais pas beaucoup dormir », a-t-il dit.
Un statisticien de Pfizer, qui était isolé du reste de l’entreprise, devait donner les nouvelles du conseil de surveillance des données par vidéoconférence.
« Nous avons eu un très bon résultat », a annoncé l’homme en début d’après-midi. Il a déclaré que Pfizer devrait immédiatement demander à la FDA de lui accorder une autorisation d’utilisation d’urgence – une mesure que la firme a prise vendredi.
La salle a éclaté sous les acclamations. Les dirigeants se sont serrés dans leurs bras, ignorant les règles de distanciation sociale.
Puis tout le monde a été évacué de la salle, sauf le Dr Bourla et l’avocat général de Pfizer, Doug Lankler, afin que les deux hommes puissent entendre la ventilation des données qui ont montré que le vaccin était efficace à plus de 95 %. Sur les 94 personnes qui étaient tombées malades, on leur a dit que 90 faisaient partie du groupe placebo et que seulement quatre faisaient partie du groupe vacciné.
« Répétez », a demandé le Dr Bourla. « Avez-vous dit 19 ou 90 ? »
« Nous avons été choqués », a-t-il dit dans l’interview. « Nous ne pouvions pas le croire. »
Ce soir-là, les responsables de Pfizer ont informé un responsable clé de la F.D.A. de sa nouvelle, ainsi qu’une courte liste d’autres personnes. L’équipe de Biden a été alertée de l’évolution de la situation ce soir-là. Mais, signe des soupçons qui marquent l’administration Trump, les hauts responsables de la santé du président n’ont appris la nouvelle que le lendemain matin, lorsqu’elle a été rendue publique.
La colère de M. Trump concernant le timing n’a pas diminué. Lors d’une conférence de presse tenue vendredi, il a laissé entendre que Pfizer et d’autres fabricants de drogue s’étaient vengés de lui pour avoir poussé le contrôle des prix de la drogue.
« Ils allaient sortir en octobre, mais ils ont décidé de retarder la sortie à cause de ce que je fais », a-t-il grommelé. « Ils ont attendu et attendu et attendu. »
Moderna a dû regarder Pfizer franchir la ligne d’arrivée en premier. Mais les résultats de Pfizer ont fait naître l’espoir dans l’entreprise.
Dimanche, en attendant les résultats du procès de Moderna, M. Bancel s’est enfermé dans un bureau à domicile dans sa maison de ville de Boston. « Je vais être une vraie loque toute la journée », a-t-il dit à sa femme.
Juste après midi, un avis a été diffusé sur le système de chat sécurisé de Moderna pour rejoindre une réunion virtuelle. Avec une douzaine d’autres membres, M. Bancel a écouté la voix plate et désincarnée d’un représentant du panel extérieur.
Les résultats ont été remarquablement semblables à ceux de Pfizer : Sur 95 infections, 90 se trouvaient dans le groupe placebo et cinq dans le groupe des vaccins.
Le panel extérieur a ensuite réparti les cas en fonction de la gravité de la maladie, une mesure essentielle de l’efficacité du vaccin.
Onze volontaires ont développé une maladie grave, a déclaré la voix. Puis vint une pause que M. Bancel dit « comme si c’était pour toujours », avant le mot final : chacun d’entre eux avait reçu le placebo.
Il s’est esquivé dans le couloir pour le dire à sa femme. Sa fille de 19 ans est descendue en courant du deuxième étage. Sa fille de 16 ans a monté les escaliers du sous-sol.
« Nous pleurions tous les quatre », a-t-il dit.
Source : (NY Times)





